2023年4月1日,CCHRPP公布了《全国GCP机构药物临床试验量值儿科排行榜》,我院药物临床试验机构跃居前五。在全国GCP机构药物临床试验量值排行榜专家工作组的指导下,中国临床研究能力提升与受试者保护高峰论坛(CCHRPP)组委会组织业内专家工作组联合行业数据公司统计分析数据形成了《CCHRPP全国GCP机构药物临床试验量值》(以下简称《试验量值》)。《试验量值》数据均来源CDE“药物临床试验登记与信息公示平台”。
《试验量值》排行榜一定程度体现了药物临床试验机构对生物医药研发的支持和助推力度,2023年度排行榜汇集2020—2022年共三年的药物临床试验实施体量,同步考量其中研发的价值指标项与权重,形成新一轮排行榜,CCHRPP始终以近三年试验数据形成榜单。
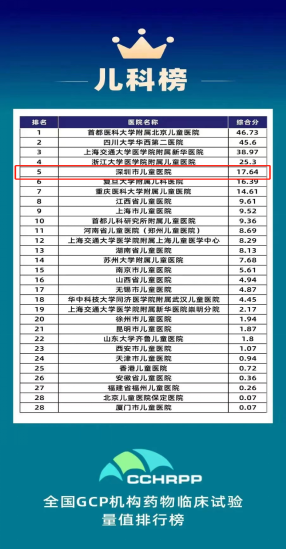
2021年度,我院药物临床试验机构在全国儿科《试验量值》排行榜中排名第十。2022年度,我院药物临床试验机构跻身全国GCP机构《试验量值》儿科排行榜八强。2023年度,我院药物临床试验机构在全国GCP机构《试验量值》儿科排行榜中跃居前五。在过去的一年里,我院药物临床试验机构克服困难,更加积极承接临床试验项目,增加人员培训,进一步提高我院研究者GCP意识,高效高质量完成临床试验项目工作。2022年,我院药物临床试验机构累计向企业提供147次临床试验服务,开展临床试验相关培训43次。截止至2022年底,我院已完成7个国家药物临床试验专业组备案,28个国家医疗器械临床试验专业组备案。2022年度,我院在研药物临床试验共64项,医疗器械临床试验共25项;新承接药物临床试验项目19项,医疗器械临床试验项目4项;完成药物临床试验3项,医疗器械临床试验2项。其余试验正在进行,且进展顺利。除服务配合专业组认真完成项目以外,2022年我院药物临床机构主要完成了以下工作:
1、迎接深圳市药品监督管理局莅临我院评估指导工作
2022年12月14日,深圳市药品监督管理局委派5名专家莅临我院,对我院医疗器械临床试验机构开展督导检查工作。院长麻晓鹏、机构主任文飞球、机构办工作人员、伦理委员会工作人员、超声诊断专业负责人、神经肌肉电图专业负责人、超声诊断专业负责人、小儿心脏病专业负责人以及PI、秘书参加首次会议。检查组专家对机构办公室、器械储存室和器械管理、人员培训、质量控制管理、伦理委员会、伦理审查等内容进行了详细检查,并对超声诊断专业、小儿心脏病专业进行了现场检查和项目检查。专家们仔细查阅了项目文件夹,检查过程中专业组对专家的提问做出了严谨、如实、全面、客观地回答。在反馈总结会议上,检查组专家对我院医疗器械临床试验工作给予了充分的肯定。
2、开展“5.20国际临床研究日”科普活动
为促进公众对于临床试验的正确认识,在第18个“国际临床研究日”,我院药物临床试验机构办公室联合伦理委员会、医技三支部党员及医技三支部所属科室团员积极响应国家儿童健康与疾病临床医学研究中心、广东省药物临床试验专委会的倡议,在住院楼一楼大厅举办以“为了儿童的未来”为主题的“5.20临床研究日科普活动”。机构主任文飞球、党办副主任王丹莅临指导。我们通过播放科普视频和家长、小朋友分享阅读《药物临床试验受试者小宝典》和儿童临床研究科普漫画《嗜睡危机》,发放“今天跟您聊聊药”“您知道新药临床试验吗?”等宣传手册、答疑等形式,让家长和小朋友正确认识临床研究,充分了解参加临床研究的权利和义务。科普活动取得了圆满成功,让大众充分地意识到临床试验的重要性,对于推进我院临床试验的开展具有重要意义。
3、成功举办广东省继续医学教育项目“儿科药物临床试验法规与技术培训”
为宣传儿科药物临床试验法规、政策及研究现状和发展,进一步提高广大医务工作者GCP意识,以及促进儿科疾病合理用药,2022年11月1日我院药物临床试验机构举办了广东省继续教育项目“儿科药物临床试验法规与技术培训”(项目编号:2022021305004)。培训班为线上线下同时举办,共520名学员参加了培训。此次省级继教培训班向学员们详细地普及了创新药物I期临床试验研究设计要点、临床试验研究者职责、儿科药物临床试验法规,以及向学员们分享了优秀药物临床试验机构管理经验。同时下午场的小儿呼吸、小儿血液、超声诊断、儿科检验、小儿神经病学专家们着重讲解了儿科疾病的合理诊治及儿科药物的合理应用。本次培训班不仅让学员充分熟悉了药物临床试验法规知识和临床试验实施过程,学员们也对儿科疾病的诊治和用药有了更深层次的了解。这次培训班极大程度地开拓了广大医务工作者的临床科研思路,为我院开展各类临床试验以及做好临床科研工作提供了指导及帮助,让医护研究者们受益匪浅。培训结束后,机构办组织学员们对儿科药物临床试验法规、理论知识等内容进行线上考核。广东省继续教育项目“儿科药物临床试验法规与技术培训”取得了圆满成功。
4、成功举办深圳市继续医学教育项目“儿科药物临床试验法规与技术培训”
为提高儿科人群药物临床研究能力,规范儿科人群药物临床试验方案设计与技术操作,增强儿科疾病安全合理用药意识,我院药物临床试验机构于2022年11月2日举办深圳市市级继续医学教育项目“儿科药物临床试验法规与技术培训班”(项目编号:22130123)。培训班开放线上及线下参会方式,共计约600人参加了本次培训。培训班立足于儿科药物研发现状和困难,介绍了儿科药物临床试验质量管理规范,分享了不同儿科疾病的诊断和治疗经验。培训结束后,学员参加了药物临床试验相关法规的线上考核。学员学习热情高涨,纷纷表示收获颇丰,不仅学习到最新的儿科药物临床试验相关政策法规,也提高了自身对于临床试验的认识。本次培训有助于增强临床试验工作者的伦理及GCP规范意识,帮助领悟GCP精神,提高临床研究能力和技术规范,提高儿科药物临床试验质量。
5、组织修订医疗器械临床试验新版管理制度
为深化医疗器械审评审批制度改革,加强医疗器械临床试验管理,国家药品监督管理局对医疗器械临床试验质量管理规范进行了修订。新版医疗器械GCP法规于2022年3月颁布,5月1日开始实施。为了保证医疗器械临床试验质量,以及进一步规范我院医疗器械临床试验管理制度,我院医疗器械临床试验机构根据2022版《医疗器械临床试验质量管理规范》,将本院医疗器械临床试验的管理规定及标准操作流程等进行了同步修订,并于2022年5月6日生效。为更新研究人员医疗器械GCP法规知识,使我院各专业组更好地承接及高质量地完成医疗器械及体外诊断试剂项目,2022年4月26日医疗临床试验机构对各专业组的研究者进行了新版医疗器械GCP培训,同时号召各专业组根据新版医疗器械GCP法规更新和完善本专业的医疗器械临床试验管理制度、规范及标准操作流程。
随着社会发展以及人们日益提高的生活水平和健康需求,同时国家与地方政府相继出台激励政策支持生物医药研发,GCP机构被列入重点支持建设对象之一。为响应科协创新发展号召,通过行业推动建立联动合作与互动支撑机制,挖掘数据价值,促进信息共建共享,创建数据服务新模式,我院药物临床试验机构在2023年度全国GCP机构药物临床试验量值儿科排行榜中位居前五,这是对我院药物临床试验工作极大的肯定,同时也激励我院研究者和管理人员不断加强自身学习,提高临床研究能力和管理水平,进而推动我国儿科药物研发,造福广大患儿。
附:迈进2023下篇|全国GCP机构药物临床试验量值排行榜盛大发布(下)