
对于有男宝的家庭来说,孩子的“丁丁”(阴茎)、“蛋蛋”(睾丸)的发育情况是家长非常关心的问题,因为二者的发育是衡量男性性发育的重要指标。如果发现孩子的“丁丁”短小、“蛋蛋”偏小甚至消失,需警惕一种名为先天性低促性腺激素性性腺功能减退症的疾病。
一、什么是“先天性低促性腺激素性性腺功能减退症”?
先天性低促性腺激素性性腺功能减退症(Congenital hypogonadotropic hypogonadism,CHH),是一种由于下丘脑在合成、分泌促性腺激素释放激素(GnRH)或者 GnRH 发挥作用时出现障碍,导致垂体分泌的促性腺激素(促黄体生成素LH和促卵泡刺激素FSH)减少,最终引起性腺功能减退的疾病。
这种疾病在孩子身上主要有这样一些表现:
第二性征不发育,如男孩可能出现“小丁丁”、“小蛋蛋”或者“蛋蛋”消失的情况
青春期延迟或无青春期发育
可能伴随无精子生成,导致不育
发病率:
国外数据:每10万人中有1~10 人发病,男性发病率是女性5倍
国内数据:目前尚无明确统计,但临床病例并不罕见
二、“蛋蛋”的一生:从出生到成年期的发育密码
蛋蛋主要由三类细胞组成(图1):
间质细胞(Leydig cells):分泌睾酮的“激素工厂”
支持细胞(Sertoli cells):为精子生成提供营养的“保姆细胞”
生殖细胞(Germ cells):未来发育成精子的“种子”
发育关键期:
出生~青春期前:蛋蛋大小主要由支持细胞数量决定
青春期:生殖细胞快速增殖和成熟,蛋蛋体积显著增大
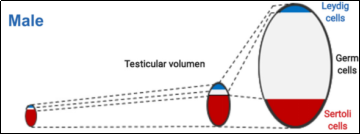
注:Testicular volume:睾丸体积;Leydig cells:间质细胞;Sertoli cells:支持细胞;Germ cells:生殖细胞
图1
三、掌管小男孩发育的“激素交响乐团”
男性性发育由下丘脑-垂体-性腺轴(Hypothalamic-pituitary-gonadal axis,HPG轴)精密调控,整个过程像一场精心编排的交响乐(图2):
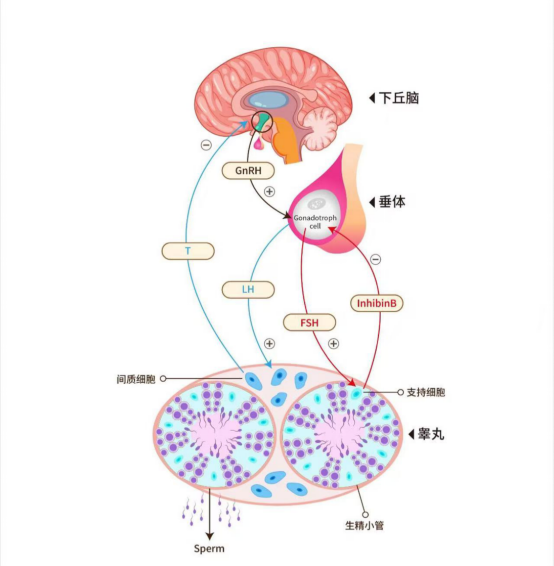
注:GnRH:下丘脑促性腺激素释放激素;LH:促黄体生成素;FSH:促卵泡刺激素;T:睾酮;InhibinB:抑制素B;Sperm:精子
图2
1.总指挥:下丘脑:
通过脉冲式释放促性腺激素释放激素(GnRH),指挥垂体工作
2.执行指挥:垂体:
分泌两种激素:
黄体生成素(LH):刺激间质细胞分泌睾酮(促进丁丁生长、变声等)
卵泡刺激素(FSH):促进支持细胞增殖(决定蛋蛋大小和精子数量上限)
3.精子工厂:睾丸:
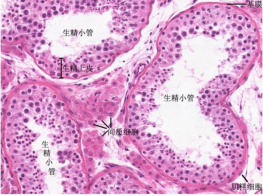
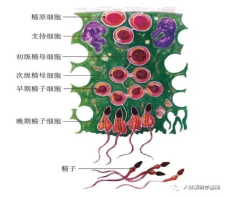
图3
最核心的“生产车间”:生精小管(图3)。
青春期,当睾丸接收到激素(如LH/FSH)的“开工指令”:
• LH刺激睾丸(蓝线)的间质细胞(Leydig细胞)产生睾酮(T)(图2)。
• 睾酮和FSH协同作用,刺激睾丸生精小管内的支持细胞(Sertoli细胞),启动和维持精子发生。
• 生殖细胞爆发式升级,通过分裂大量增殖,逐步变形成蝌蚪状的精子。
4.三大发育关键时期(HPG轴的三个活跃时期):
四、CHH患者的不同命运:GnRH的多种异常模式(图4)
根据GnRH分泌特点,CHH可分为以下类型:
1. 完全性缺陷:从胎儿期/婴儿期就彻底“停工”(2/3型)
2. 部分性缺陷:激素分泌“偷懒”,仅维持最低水平(4型)
3. 成年发病型:青春期正常发育,成年后突然“罢工”(5型)
部分患者可能出现GnRH分泌“反复无常”的特殊情况(2A/3A/2B型)
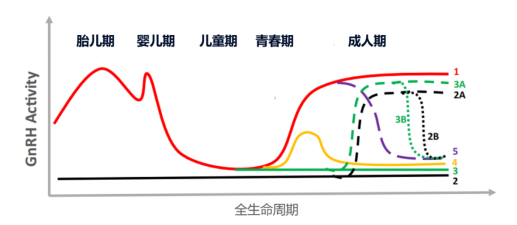
图4
五、年龄不同,治疗重点不同
CHH治疗需“量体裁衣”,但核心目标始终是:保护生育力,模拟正常发育节奏。
给家长的重要提示
1. 早发现:若孩子生后丁丁短小(小于2.5厘米)和(或)蛋蛋未下降,或14岁仍无发育迹象,尽早就诊
2. 别焦虑:即使确诊CHH,通过规范治疗,多数患者可正常发育并生育
3. 慎用药:任何激素治疗都需在专业医生指导下进行,切勿自行用药
(注:文中示意图可帮助理解激素调控机制和疾病分型,具体诊断需结合临床检查)